با اشتراک در خبرنامه همیشه از آخرین تخفیفات و رویدادهای مهم ما مطلع خواهید شد
آمونیوم پرکلرات چیست؟
آمونیوم پرکلرات (Ammonium Perchlorate) یک ترکیب شیمیایی با فرمول NH₄ClO₄ است که به طور گستردهای به عنوان اکسیدکننده در سوختهای موشکی جامد استفاده میشود. این ماده به شکل پودر سفید رنگ وجود دارد و به دلیل خصوصیات اکسیدکننده قوی خود، یکی از اجزای اصلی سوختهای موشکی جامد است.
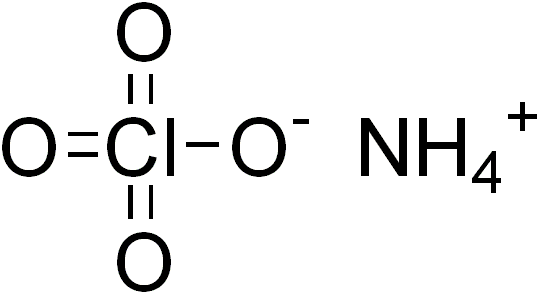
ویژگیها و کاربردها:
1. **اکسیدکننده قوی:**
آمونیوم پرکلرات به عنوان یک اکسیدکننده قوی عمل میکند که میتواند با مواد سوختی ترکیب شود و در نتیجه احتراق قوی و پرانرژی ایجاد کند. این خصوصیت آن را به یک ماده مهم در صنایع هوافضا و نظامی تبدیل کرده است. در طول جنگ جهانی اول انگلستان و فرانسه از مخلوط های حاوی پرکلرات آمونیوم (مانند "بالستین") به عنوان جایگزین مواد منفجره استفاده کردند.
هنگامی که آمونیوم پرکلرات با یک سوخت (مانند آلومینیوم پودری و/یا با چسب الاستومری) مخلوط میشود، میتواند احتراق خودپایهای را در فشارهایی بسیار کمتر از فشار اتمسفر ایجاد کند. این یک اکسید کننده مهم با سابقه چندین دهه استفاده در پیشرانه های موشک جامد - پرتاب فضایی (از جمله تقویت کننده موشک جامد شاتل فضایی)، موشک های پرقدرت نظامی، آماتوری و سرگرمی و همچنین در برخی آتش بازی ها است.
2. **پایداری حرارتی:**
آمونیوم پرکلرات دارای پایداری حرارتی بالایی است که این ویژگی آن را برای استفاده در محیطهای سخت و دمای بالا مناسب میکند. این ویژگی به خصوص در موشکهای بالستیک و فضاپیماها مهم است.
3. **ایمنی و ذخیرهسازی:**
این ماده نسبت به بسیاری از اکسیدکنندههای دیگر ایمنتر است و میتواند برای مدت طولانی بدون خطر نگهداری شود. با این حال، در صورت ترکیب با سوختهای مناسب، بسیار قابل اشتعال و انفجار است.
4. **کاربردها:**
- **سوختهای موشکی جامد:** آمونیوم پرکلرات به طور گستردهای در ترکیب با سوختهای پلیمر مانند HTPB (هیدروکسیل-ترمینیتد پلیبوتادین) استفاده میشود. این ترکیب به عنوان سوخت جامد در موشکهای نظامی و همچنین در برخی از پرتابگرهای فضایی استفاده میشود.
- **پیرودوستاتها و مواد آتشبازی:** این ماده همچنین در ساخت پیرودوستاتها (مواد آتشزا) و مواد آتشبازی استفاده میشود.
فرآیند تولید:
تولید آمونیوم پرکلرات به طور عمده از طریق واکنش بین آمونیوم کلرید و سدیم پرکلرات انجام میشود.
NaCLO4 + NH4Cl ---> NaCl+NH4CLO4
این واکنش در شرایط کنترل شده انجام میشود تا محصول خالص و با کیفیت به دست آید.

تجزیه
مانند اکثر نمک های آمونیوم، پرکلرات آمونیوم قبل از ذوب تجزیه می شود. حرارت ملایم منجر به تولید کلرید هیدروژن، نیتروژن، اکسیژن و آب می شود.
4 NH4ClO4 → 4 HCl + 2 N2 + 5 O2 + 6 H2O
احتراق آمونیوم پرکلرات بسیار پیچیده است و به طور گسترده مورد مطالعه قرار گرفته است. کریستال های AP قبل از ذوب تجزیه می شوند، حتی اگر یک لایه مایع نازک بر روی سطوح کریستال در طی فرآیندهای احتراق با فشار بالا مشاهده شده است. گرمای شدید ممکن است منجر به انفجار شود. واکنش های کامل هیچ اثری باقی نمی گذارد. کریستال های خالص نمی توانند شعله ای را زیر فشار 2 مگاپاسکال نگه دارند.
نکات ایمنی:
در هنگام کار با آمونیوم پرکلرات باید نکات ایمنی رعایت شود. این ماده باید در ظروف محکم و دور از مواد قابل اشتعال و حرارت نگهداری شود. استفاده از تجهیزات حفاظتی مانند دستکش و ماسک در هنگام کار با این ماده ضروری است.
سمیت
پرکلرات به خودی خود سمیت حاد کمی ایجاد می کند. مواجهه مزمن با پرکلرات ها، حتی در غلظت های پایین، باعث ایجاد مشکلات مختلف تیروئید می شود، زیرا به جای ید جذب می شود.
آمونیوم پرکلرات یک ماده حیاتی در صنعت هوافضا و نظامی است که با توجه به خصوصیات منحصر به فرد خود، نقش مهمی در توسعه فناوریهای پیشرفته دارد.


