با اشتراک در خبرنامه همیشه از آخرین تخفیفات و رویدادهای مهم ما مطلع خواهید شد
مروری بر نیترات پتاسیم
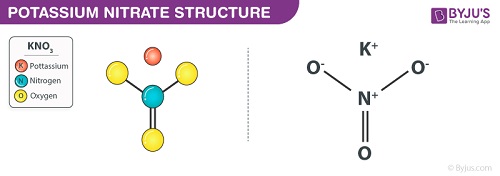
نیترات پتاسیم به یک ترکیب با فرمول شیمیایی KNO3 است. این یک ترکیب متبلور سفید است. نیترات پتاسیم به نمک پتاسیم کریستالی، بی رنگ و اسید نیتریک اشاره دارد. از پتاسیم، نیتروژن و اکسیژن تشکیل شده است. علاوه بر این، این ترکیب کاربرد قابل توجهی در آتش بازی، کبریت و کود شیمیایی داشته و همچنین در مقاصد پزشکی مانند دیورتیک ها برای کاهش فشار خون استفاده می شود.
از نظر تاریخی، این ترکیب نخست از رسوبات دیواره غار برداشت شده است. این رسوبات دیواری دارای تجمعی از گوانو خفاش بودند. این ترکیب به طور کلی نمک بی خطر است. علاوه بر این، این ترکیب در دوزهای متوسط باعث تحریک در بینی و گلو می شود. مردم از قرون وسطی از آن به عنوان نگهدارنده مواد غذایی استفاده می کردند. علاوه بر این، این نمک در باروت، آتش بازی، کبریت و پودرهای انفجار وجود دارد. این ترکیب در سوخت موشک وجود داشته و در صنایع فولاد و ساخت شیشه بسیار مفید است.
خمیر دندان های حساس و محصولات سفید کننده دندان مطمئناً حاوی این ترکیب هستند. علاوه بر این، نیترات پتاسیم در پرایمر مواد آرایشی وجود دارد. این ترکیب مطمئناً در تحقیقات دندانپزشکی کاربرد دارد. علاوه بر این، صنایع شیمیایی برای حفظ دما به شدت به نیترات پتاسیم متکی است.
نیترات پتاسیم در کودهای مختلف، مخلوط گلدانی و غذاهای گیاهی نیز کاربرد گسترده ای دارد. بخورهای پیروتکنیک حاوی این ترکیب برای کنترل حشرات، جوندگان و انواع مختلف آفات هستند. علاوه بر این، این کارتریج ها گازهای کشنده آفات را برای کنترل کایوت ها، اسکنک ها، زنبورها و سایر حیواناتی که برای محصولات زراعی و مزارع مضر هستند ایجاد می کنند. به دلیل وجود پتاسیم در طبیعت، این ترکیب ممکن است برخی از اثرات زیست محیطی را ایجاد کند. این ترکیب همچنین در بسیاری از کودها موجود است و بنابراین برای کشاورزی مفید است.
نیترات پتاسیم در تولید انرژی های تجدیدپذیر بسیار پرکاربرد است و یک عنصر بسیار مهم در نمک خورشیدی به شمار می رود. نمک خورشیدی به نمک مذابی گفته می شود که به عنوان ذخیره گرما در نیروگاه های خورشیدی عمل می کند.

نیترات پتاسیم در دمای عادی از یک ساختار کریستالی متعامد تشکیل شده است. این ساختار در دمای 129 درجه سانتیگراد به یک سیستم مثلثی تبدیل می شود. نیترات پتاسیم مطمئناً به طور متوسط در آب محلول است. با این حال، حلالیت آن با دما افزایش می یابد.
محلول آبی نیترات پتاسیم تقریبا خنثی است، که pH 6.2 را در 14 درجه سانتیگراد نشان می دهد. ماهیت آن خیلی مرطوب نیست ولی حدودا 0.03 درصد آب را طی 50 روز در رطوبت نسبی 80 درصد جذب می کند. نیترات پتاسیم در الکل نامحلول است. علاوه بر این، این ترکیب سمی نیست.
نیترات پتاسیم با خنثی کردن اسید نیتریک با هیدروکسید پتاسیم یا کربنات پتاسیم و تبخیر محلول حاصل رسوب میکند. نیترات پتاسیم نیز از واکنش کلرید پتاسیم با اسید نیتریک غلیظ تولید می شود.

هنگامی که نیترات پتاسیم بالاتر از دمای ذوب 339 درجه سانتیگراد گرم می شود، اکسیژن می دهد و به نیتریت پتاسیم تبدیل می شود. نیترات پتاسیم همچنین یک اکسید کننده قوی است و در صورت واکنش با سایر ترکیبات آلی می تواند انفجاری باشد. با این حال، این ترکیب به خودی خود انفجاری نیست.
از نظر تاریخی، این ترکیب نخست از رسوبات دیواره غار برداشت شده است. این رسوبات دیواری دارای تجمعی از گوانو خفاش بودند. این ترکیب به طور کلی نمک بی خطر است. علاوه بر این، این ترکیب در دوزهای متوسط باعث تحریک در بینی و گلو می شود. مردم از قرون وسطی از آن به عنوان نگهدارنده مواد غذایی استفاده می کردند. علاوه بر این، این نمک در باروت، آتش بازی، کبریت و پودرهای انفجار وجود دارد. این ترکیب در سوخت موشک وجود داشته و در صنایع فولاد و ساخت شیشه بسیار مفید است.

خمیر دندان های حساس و محصولات سفید کننده دندان مطمئناً حاوی این ترکیب هستند. علاوه بر این، نیترات پتاسیم در پرایمر مواد آرایشی وجود دارد. این ترکیب مطمئناً در تحقیقات دندانپزشکی کاربرد دارد. علاوه بر این، صنایع شیمیایی برای حفظ دما به شدت به نیترات پتاسیم متکی است.
نیترات پتاسیم در کودهای مختلف، مخلوط گلدانی و غذاهای گیاهی نیز کاربرد گسترده ای دارد. بخورهای پیروتکنیک حاوی این ترکیب برای کنترل حشرات، جوندگان و انواع مختلف آفات هستند. علاوه بر این، این کارتریج ها گازهای کشنده آفات را برای کنترل کایوت ها، اسکنک ها، زنبورها و سایر حیواناتی که برای محصولات زراعی و مزارع مضر هستند ایجاد می کنند. به دلیل وجود پتاسیم در طبیعت، این ترکیب ممکن است برخی از اثرات زیست محیطی را ایجاد کند. این ترکیب همچنین در بسیاری از کودها موجود است و بنابراین برای کشاورزی مفید است.
نیترات پتاسیم در تولید انرژی های تجدیدپذیر بسیار پرکاربرد است و یک عنصر بسیار مهم در نمک خورشیدی به شمار می رود. نمک خورشیدی به نمک مذابی گفته می شود که به عنوان ذخیره گرما در نیروگاه های خورشیدی عمل می کند.

نیترات پتاسیم در دمای عادی از یک ساختار کریستالی متعامد تشکیل شده است. این ساختار در دمای 129 درجه سانتیگراد به یک سیستم مثلثی تبدیل می شود. نیترات پتاسیم مطمئناً به طور متوسط در آب محلول است. با این حال، حلالیت آن با دما افزایش می یابد.
محلول آبی نیترات پتاسیم تقریبا خنثی است، که pH 6.2 را در 14 درجه سانتیگراد نشان می دهد. ماهیت آن خیلی مرطوب نیست ولی حدودا 0.03 درصد آب را طی 50 روز در رطوبت نسبی 80 درصد جذب می کند. نیترات پتاسیم در الکل نامحلول است. علاوه بر این، این ترکیب سمی نیست.
نیترات پتاسیم با خنثی کردن اسید نیتریک با هیدروکسید پتاسیم یا کربنات پتاسیم و تبخیر محلول حاصل رسوب میکند. نیترات پتاسیم نیز از واکنش کلرید پتاسیم با اسید نیتریک غلیظ تولید می شود.

هنگامی که نیترات پتاسیم بالاتر از دمای ذوب 339 درجه سانتیگراد گرم می شود، اکسیژن می دهد و به نیتریت پتاسیم تبدیل می شود. نیترات پتاسیم همچنین یک اکسید کننده قوی است و در صورت واکنش با سایر ترکیبات آلی می تواند انفجاری باشد. با این حال، این ترکیب به خودی خود انفجاری نیست.


